水溶液中では、単糖類であるグルコース、フルクトース、ガラクトースは平衡状態にあって還元性を示します。
中でもフルクトースは、六員環構造のα−フルクトース・β−フルクトース、鎖状構造、五員環構造のα−フルクトース・β−フルクトースの、5つの平衡状態で存在しています。
今回は、「混成軌道」の記事で紹介致しましたフルクトースを中心に、再度こちらの記事で単糖類として紹介していきたいと思いますので、どうぞお付き合い下さい!
混成軌道の記事については、是非こちらを御覧下さい!
「必見!酢酸CH3COOHの2s軌道が電子0個になる謎とは!?」
1.フルクトース(果糖)の性質!

また甘味の強度は、フルクトース≫グルコース≫ガラクトースであり、酵素チマーゼによってアルコール発酵可能となります。
この様にアルコール発酵させるとエタノールC2H5OHと二酸化炭素CO2が生成されます。
「アルコール発酵と言えば、多糖類であるデンプン・セルロース・グリコーゲンを加水分解して単糖類にしてから酵素によってアルコール発酵させ、エタノールC2H5OHと二酸化炭素CO2が生成される!」とイメージして頂けたらと思います。
2.グルコースとガラクトースの構造と平衡状態!
ここでフルクトースの平衡状態に関係の深い、グルコースとガラクトースの構造と平衡状態について触れておきましょう。
グルコースとガラクトースの構造は、非常によく似ています。4位に着く、−H基と−OH基が逆になっているだけです。この状態で平衡状態となりアルデヒド基−CHOによって還元性を示します。
まずは、グルコースの平衡状態について考えてみましょう。
2−1.グルコースの平衡状態!
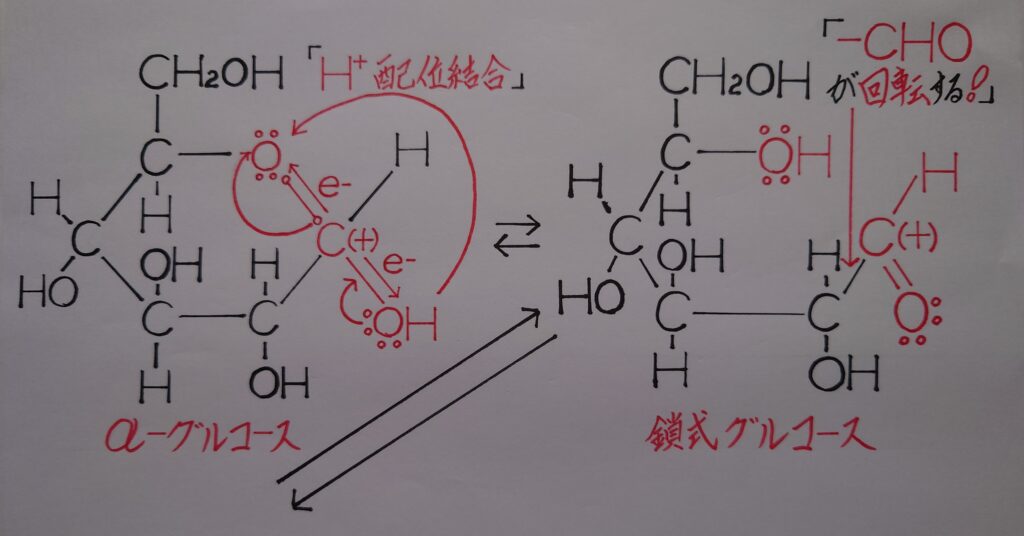
このヘミアセタールの酸素原子Oとヒドロキシ基−OHの酸素原子Oが炭素原子Cを電気陰性度の差によって強く引き付けると、炭素原子Cは正(+)に偏った状態になっています。このC(+)がヒドロキシ基−OHのOの非共有電子対(ローンペア)を引き付けて二重結合を形成するとケトン基・〉C=OのOがO^+となり、これと水素イオンH^+とが反発し合いH^+が弾かれます。
更にここで炭素原子Cがオクテット則(8電子則)を満たさなくなった為に、Cと結合しているもう1つの酸素原子Oとの結合が切れCの1電子がOに奪われO^-と負(−)に帯電します。ここに先程脱離した水素イオンH^+が配位結合し、鎖式グルコースが生成されアルデヒド基−CHOを形成します。
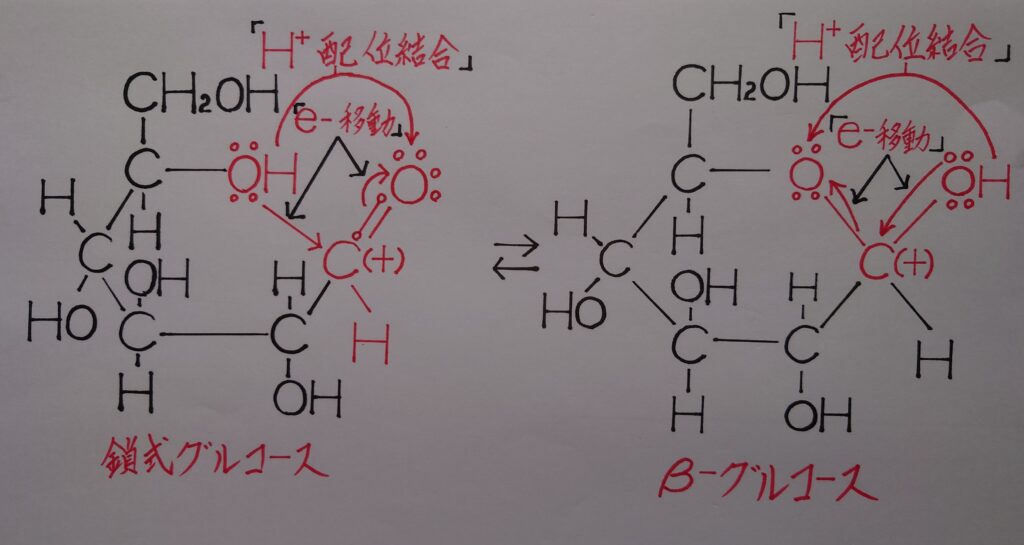
このアルデヒド基−CHOは1位の炭素原子Cを中心に回転出来る為、もう1つの鎖式グルコースが生成され平衡状態に入ります。この2つ目の鎖式グルコースのヒドロキシ基−OHの酸素原子Oの非共有電子対(ローンペア)をC(+)が引き付けて共有結合を形成します。
ここで炭素原子Cがオクテット則を満たす為に、二重結合のケトン基・〉C=Oのπ電子が完全にO側の電子となりO^-となります。そしてO^-にヒドロキシ基−OHの水素イオンH^+が配位結合しβ−グルコースが生成する、といった平衡状態となります。皆さん、うまくイメージ出来たのではないでしょうか!
2−2.ガラクトースの平衡状態!
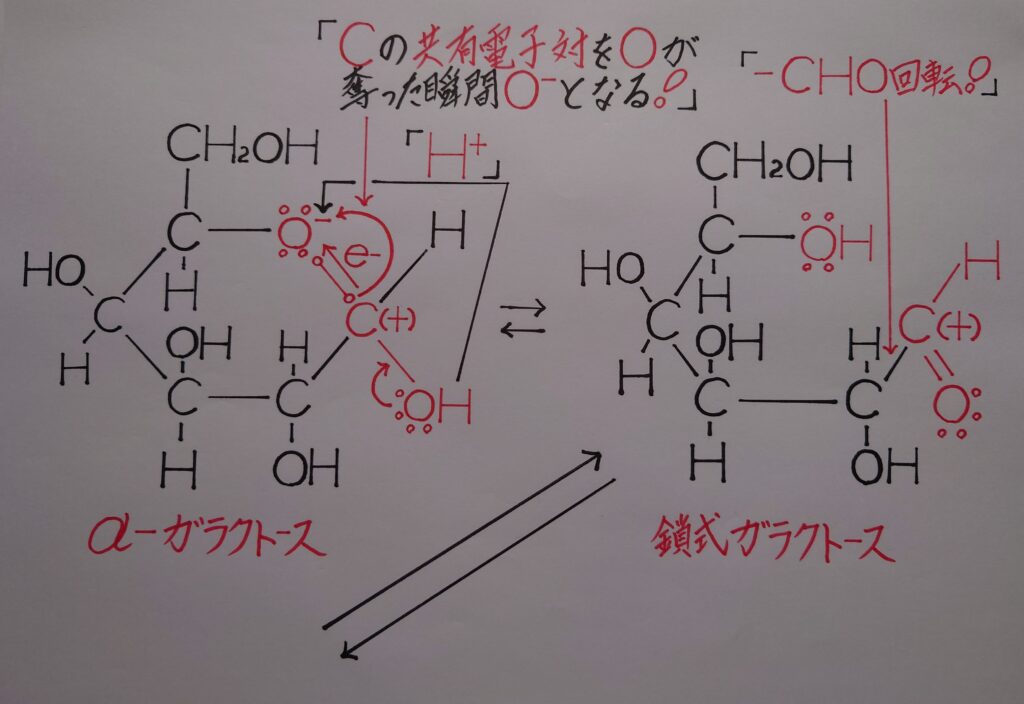
このヘミアセタールの炭素原子Cは酸素原子Oとヒドロキシ基−OHのOに電気陰性度の差によって引き付けられており、正電荷(+)に偏っています。この正(+)に偏ったCは酸素原子Oとの共有電子対ごと奪われOはO^-となります。
逆に電子を奪われたCは「❋ カルボカチオンC^+」(❋ 画像中にはカルボカチオンC^+は書いていませんが、反応中に生成されていますのでイメージされたらと思います。なお、グルコースの場合も同様です!)となりヒドロキシ基−OHのOの非共有電子対を引き付けて奪いπ結合となる二重結合を形成します。
そしてOが正(+)に帯電する為に水素原子Hが水素イオンH^+として反発し合いH^+が脱離し、脱離後O^-に配位結合し鎖式ガラクトースなりα−ガラクトースと平衡状態に入ります。この時、還元性を示すアルデヒド基−CHOが生成されますが、これは回転する事が可能になっています。
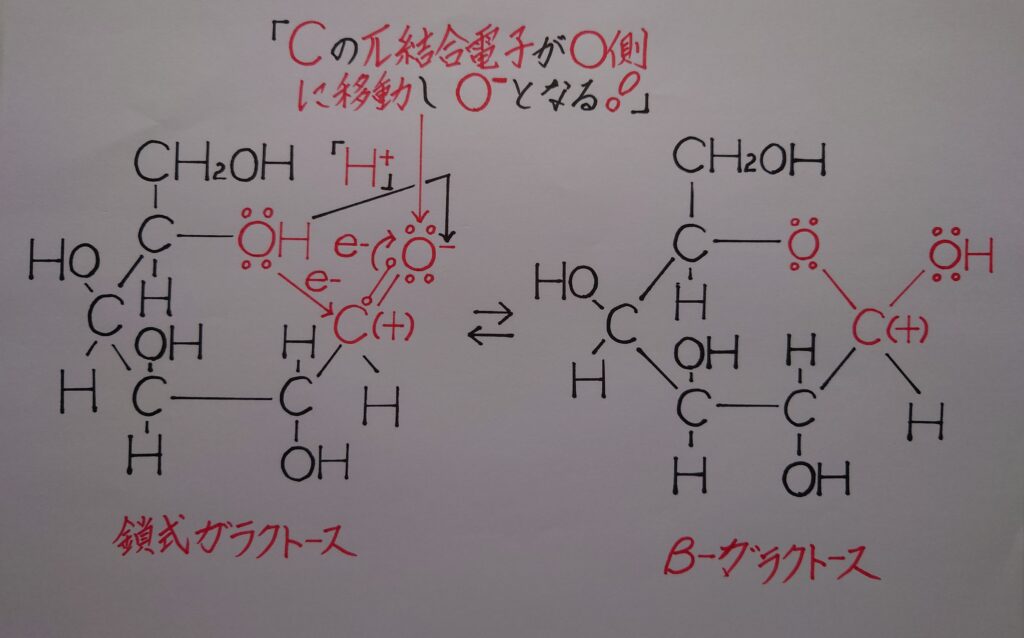
次に、この回転したアルデヒド基−CHOが動き出します。アルデヒド基−CHOの正(+)に偏っているC(+)が、先程のヒドロキシ基−OHのOのローンペアを奪い引き付けてOと共有結合を形成します。
Oと共有結合を形成したC(+)はオクテット則(8電子則)を満たさなくなった為に、結合の弱いC=O間のπ結合の電子がO側に完全に移動しなければならずO^-の負(−)として帯電します。
そして、先程ローンペアを失ったOが正(+)に帯電する為に、水素原子Hが水素イオンH^+として反発し合い弾かれると、アルデヒド基−CHOのO^-に配位結合しβ−ガラクトースが生成され平衡状態に入ります。
考え方と致しましては、ヘミアセタール・O−C−OHを中心にグルコースの平衡状態と同じ考え方ですので、理解しやすかったのではないでしょうか!
3.フルクトースの構造と平衡状態!
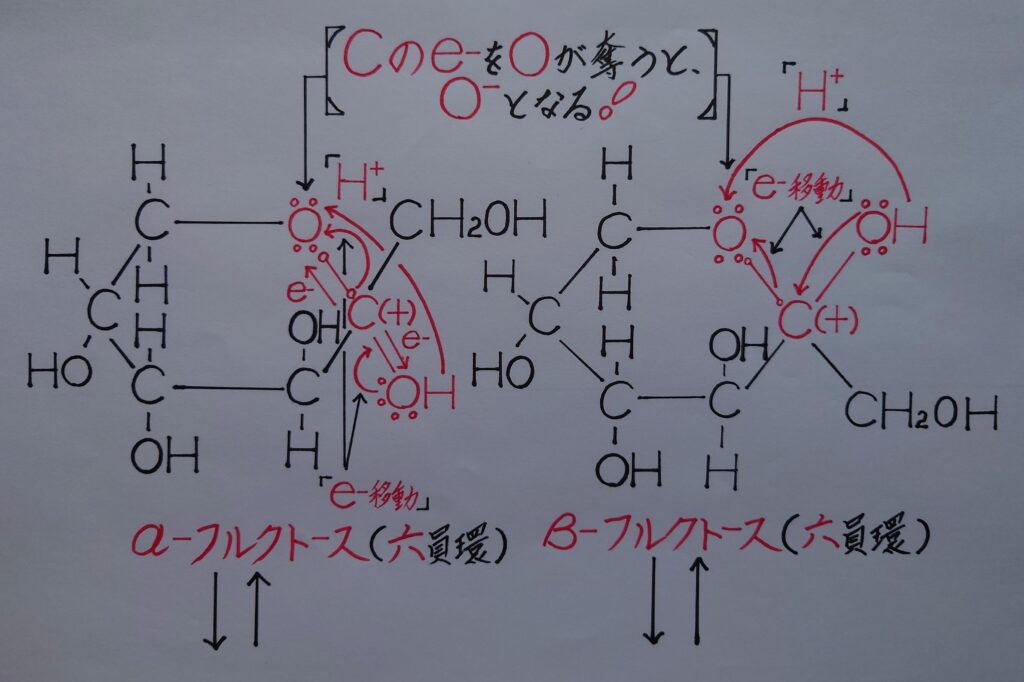

フルクトースの平衡状態に付きましては、上画像の様な「❋ 六員環構造のα−フルクトースとβ−フルクトース、2種類の鎖状構造のフルクトース、五員環構造のα−フルクトースとβ−フルクトース!」から成り立っています。
皆さん4つの画像から、おおよその平衡状態は理解出来るとは思いますが、再度1つ1つの画像について分けて考えていきたいと思います。

フルクトース(六員環)にもグルコース、ガラクトースと同様に「❋ ヘミアセタール・O−C−OH」が存在します。
まずα−フルクトース(六員環)、β−フルクトース(六員環)ですが、フルクトースのヘミアセタール・O−C−OHがグルコース、ガラクトースと同じ動きによって2種の鎖式フルクトースが生成し平衡状態となります!

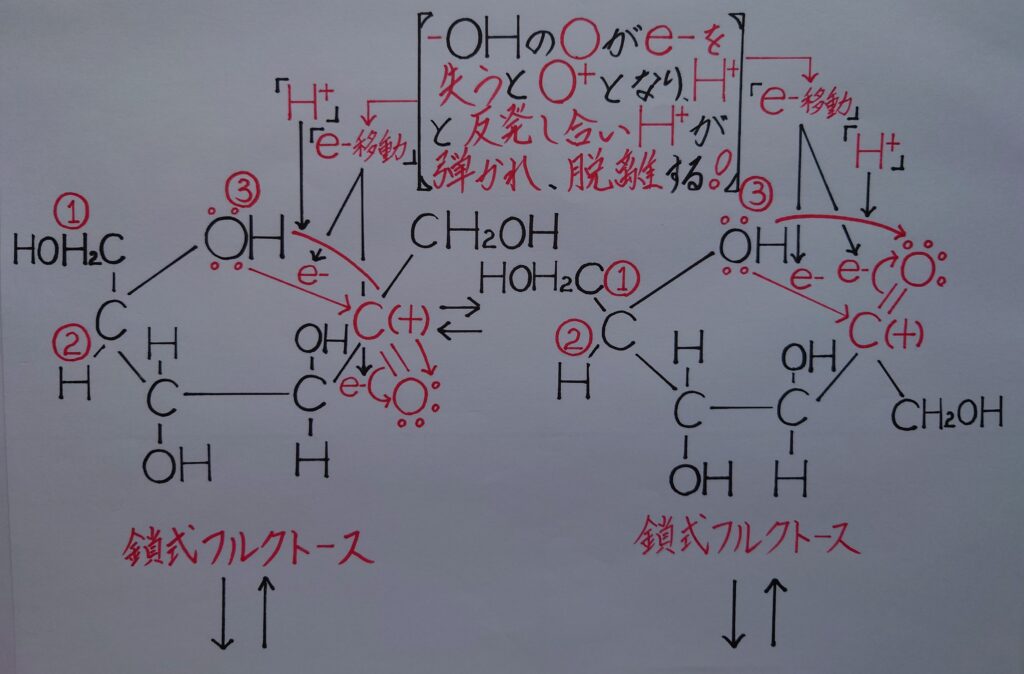
2種の鎖式フルクトースは平衡状態に在りますが、これは−CO−CH2OHのC(+)の部分が回転するからです。そして画像の2つの(1)、(2)、(3)の中心にあります2つの「❋ 5位の炭素原子C」が−OH方向に回転すると、2種の五員環の様な鎖式フルクトースが生成され平衡状態となります!

ここでは、この鎖式フルクトースのてっぺんの−OH基のOの非共有電子対を正(+)に偏ったC(+)が引き付けて共有結合を形成します。そしてこの瞬間、−OH基のOが1電子を失った為に正(+)に帯電しO^+となり、水素原子Hが水素イオンH^+としてO^+と反発し合って脱離します。
さらにオクテット則を満たさなくなったC(+)が電子を吸収した際に、ケトン基・〉C=OのOのπ電子をO側に完全に追いやり負(−)に帯電しO^-となります。このO^-に先程脱離したH^+が配位結合し、α−フルクトース(五員環)とβ−フルクトース(五員環)が生成し、鎖式フルクトースと平衡状態に入ります!

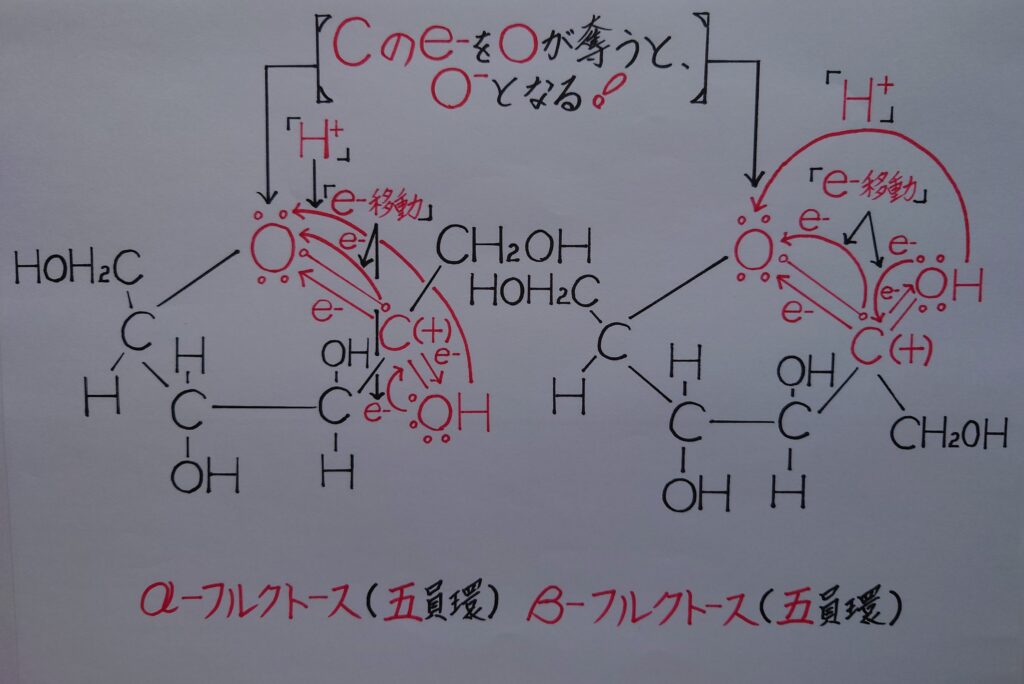
α−フルクトース(五員環)とβ−フルクトース(五員環)が生成すると、五員環のてっぺんのO原子がC(+)との共有電子対ごと電子を奪いO^-となります。電子を奪われたC(+)はカルボカチオンC^+となり、−OH基のO原子の非共有電子対を吸収しOと二重結合を形成します。
電子が奪われたOはO^+として正(+)に帯電する為に、水素原子Hが水素イオンH^+として反発し合い弾かれると、てっぺんのO^-に配位結合し−OH基を形成し、鎖式フルクトースと平衡状態に入ります。
後は、4つの画像全てが互いに平衡状態に入る様(さま)をイメージして頂けたらと思います!
皆さん、うまくイメージ出来たのではないでしょうか?結局、フルクトースの中にヘミアセタール・O−C−OHが存在しますので、グルコース、ガラクトースと同様に考えて頂けたらと思います。
また、酸素原子O(❋ −OH基のOも含む!)の所有する非共有電子対(ローンペア)と、ケトン基・〉C=Oの所有する二重結合(π結合)のπ電子の存在にも着目して頂けたら理解度がアップするのではないでしょうか!
3−1.フルクトースは、R−CO−CH2OH構造の平衡状態に還元性を示すアルデヒド基−CHOを所有する!
ですが、水溶液中でのフルクトース、グルコース、ガラクトースには共通点があります。それが混成軌道の記事内で紹介致しました、「❋ 水溶液は銀鏡反応を示し、フェーリング液を還元するが、これ等は条件として平衡状態にある鎖状構造のアルデヒド基−CHOが存在しなければならない!」という共通点です。
しかし、平衡状態にある鎖状構造を観ると、グルコースとガラクトースにはアルデヒド基−CHOがあり還元性を示す事が解りますが、フルクトースの鎖状構造にはアルデヒド基−CHOが無いように思えます。
今回フルクトースを中心に単糖類を題材として設けたのは、「❋ フルクトースの平衡状態が理解しづらい!」事と、フルクトースの平衡状態において鎖状構造にある時は、「❋ R−CO−CH2OHの構造を所有しており、この構造が更に平衡状態となってアルデヒド基−CHOが出現し還元性を示す!」事から、再度画像によって理解して頂きたいと思い記事と致しました!
3−2.フルクトース・R−CO−CH2OHの構造の平衡状態!

上画像はフルクトースが水溶液中で平衡状態にある時を表しています。この平衡状態の原子間の結合に着目して観ると、二重結合が移動しているのが解ります。通常フルクトースの平衡状態はこの様に表してありますが、これだけでは理解しづらく思えます。
そこで、平衡状態をもっと詳しく表した画像が次の様になっています。
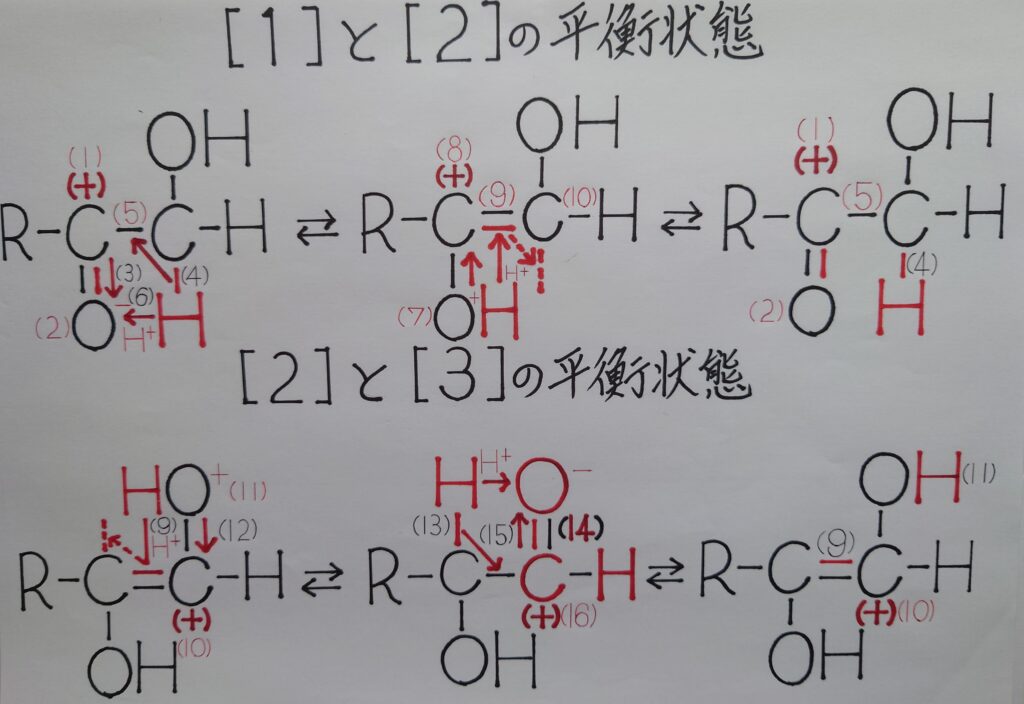
【❋ 幾つか画像内に炭素原子C(+)として存在していますが、このCは酸素原子Oに電気陰性度の差から電子を引き付けられ正(+)に偏って帯電しているだけで、電子1個を奪われた正電荷(+)のカルボカチオンC^+ではない事を理解しておいて下さい!】
1番目の画像では中々理解出来ない事も、2番目の画像ではどの様に二重結合であるπ電子が移動しているのかが理解出来たのではないでしょうか!
またカルボカチオンC^+の様な働きをして原子が移動する平衡状態は、「❋ ケト−エノール互変異性!」と呼ばれる反応によく似ています。いえ、反応そのものと言っても過言ではないと思います。
フルクトースの様に炭素原子Cの隣に酸素原子Oが存在している場合、この様な反応も起こりやすいと覚えておいて下さればフルクトースの平衡状態も理解しやすいでしょう。
更に平衡状態における5員環と6員環が何故存在するのかイメージしやすくなるでしょう。
今回は、グルコース、ガラクトース、フルクトースの平衡状態及びフルクトースのアルデヒド基−CHOが還元性を示す詳細に触れて来ました。皆さん再確認されたのではないでしょうか?
単糖類は互いに構造が非常によく似ており、様々な要素によって単糖類の平衡状態は成立しています。特にフルクトースの平衡状態は色々な反応に応用化出来る場面も出て来る可能性がありますので、会得されたらと思います。
またグルコース、フルクトース、ガラクトースの構造についても、構造の左側から右側の方向にヒドロキシ基−OHの位置だけを中心に覚えて頂けたらと思います。あまり難しく考えない事をおすすめします。
さて、皆さん今回もお付き合い下さいまして誠に有難う御座いました。別記事も是非御閲覧頂けたらと思います。それでは、この辺で See you!




















