大袈裟なタイトルと皆さん思われたでしょうが、今回はフェノール(❋ 言わば副産物としてアセトンも生産されます!)が工業的に生産される製法の中で最も代表的な「クメン法の一連有機反応機構!」について進めて行きたいと思います。
実はクメン法、タイトル通り単純な作業でフェノールが製法される訳ではないんです。起承転結の言葉みたいに様々な反応を段階的に践みながら最終的にフェノールとアセトンが生成されるんです。言わば芳香族の集大成と言っても過言ではない!程反応の過程がややこしいんです。
ですが、ややこしいからこそ皆さんのイメージトレーニングにうってつけの材料になると思いますので、反応の名称等から1つ1つ確実に理解しながらフェノールの生成迄辿り着きましょう。
【✺ クメン法の他に、クロロ化・ニトロ化・スルホン化+ジアゾカップリングの記事も是非御覧下さい!】
「これぞ明解!ベンゼンから、クロロベンゼンが誕生する仕組み!」
「上級名答!ベンゼンから、ニトロベンゼンが誕生する仕組み!」
「絶対太鼓判!ベンゼンからベンゼンスルホン酸が誕生する仕組み!」
それではスタート致しましょう!
1.ベンゼンC6H6とプロピレン(プロペン)C3H6の反応から始まるクメン法!

しかし、プロピレンは正(+)に偏っている、又は正電荷(+)の分子ではないのでベンゼンの負(−)の6π電子雲と互いに引き寄せ合う事が出来ません。
そこでプロピレンC3H6を、「CH2=CH−CH3」として考えますと、アルケン(❋ 電子余剰分子としてπ電子が余っている状態で求核剤と呼ばれ、生成反応図ではNuと省略されます!)として分子中に二重結合を形成しており、π結合によるπ電子が存在している事に気付きます。
このπ電子を利用してプロピレンを正電荷(+)にしてしまうと6π電子雲に近づく事が可能になります。それにはプロピレンのπ電子と「❋ 酸であるH^+!」とを付加反応として発動させなければなりません。つまりπ電子に酸H^+(プロトン)を付加させる事で、プロピレン分子内は正(+)に帯電する事になります。
この重要となります最初の第1段階の反応を「❋ マルコフニコフ則!」と呼んでいます!
2.マルコフニコフ則によるカルボカチオンの生成!
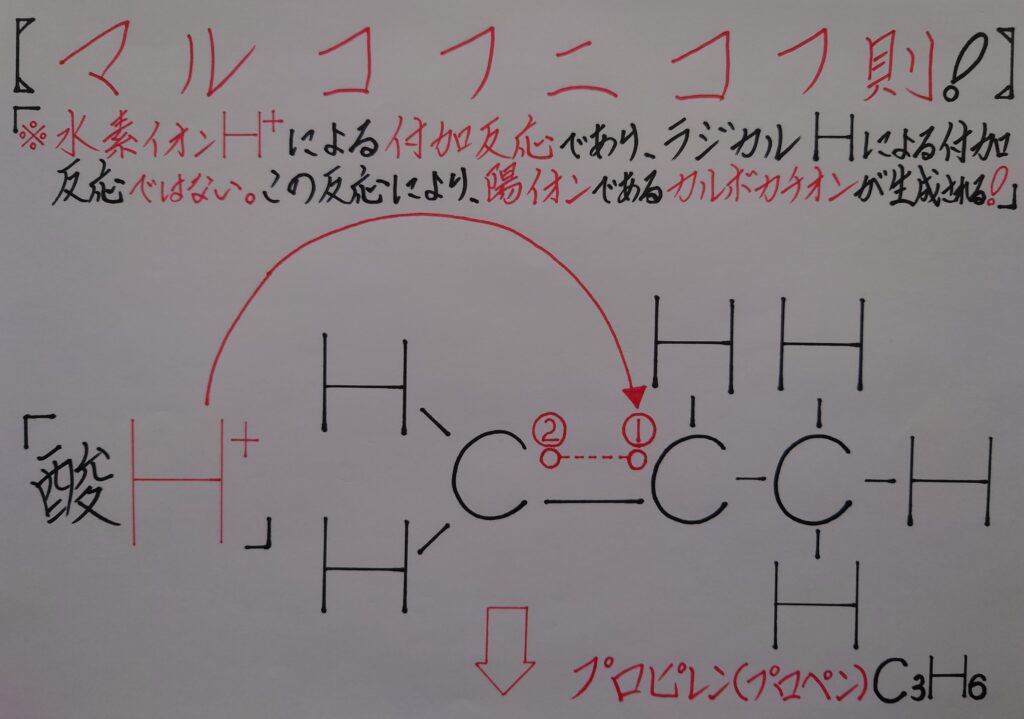
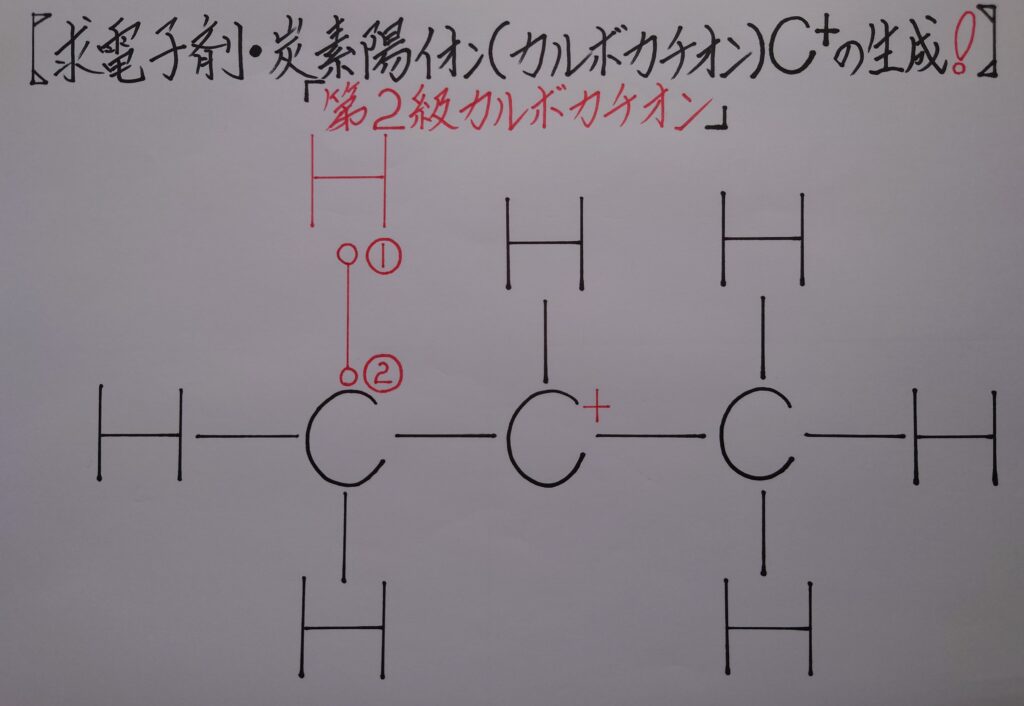
このプロピレン分子の中央部分の炭素原子Cが左右のアルキル基とσ結合を形成し第2級炭素陽イオン(第2級カルボカチオン)となる事で、最も安定した陽イオンの求電子剤が生成する事になります。
マルコフニコフ則により陽イオンであるカルボカチオンが求電子剤となる事により、ここから下の3.画像のベンゼンとカルボカチオンとが互いに引き寄せ合い、6π電子雲の(1)の1π電子を奪うとイプソ位に位置する炭素原子Cは炭素陽イオンC^+となり、次いで(2)に残っている1π電子を奪い、ここでベンゼンとプロピレンが一旦σ結合を形成します。
第2段階の反応として、ベンゼンとプロピレンのσ結合による中間体C6H6CH(CH3)2^+を経て、イソプロピル基を所有するクメンC6H5CH(CH3)2(イソプロピルベンゼン)が生成される反応を、「❋ フリーデル・クラフツ反応!」と呼んでいます!
3.フリーデル・クラフツ反応によりクメンを生成させる!
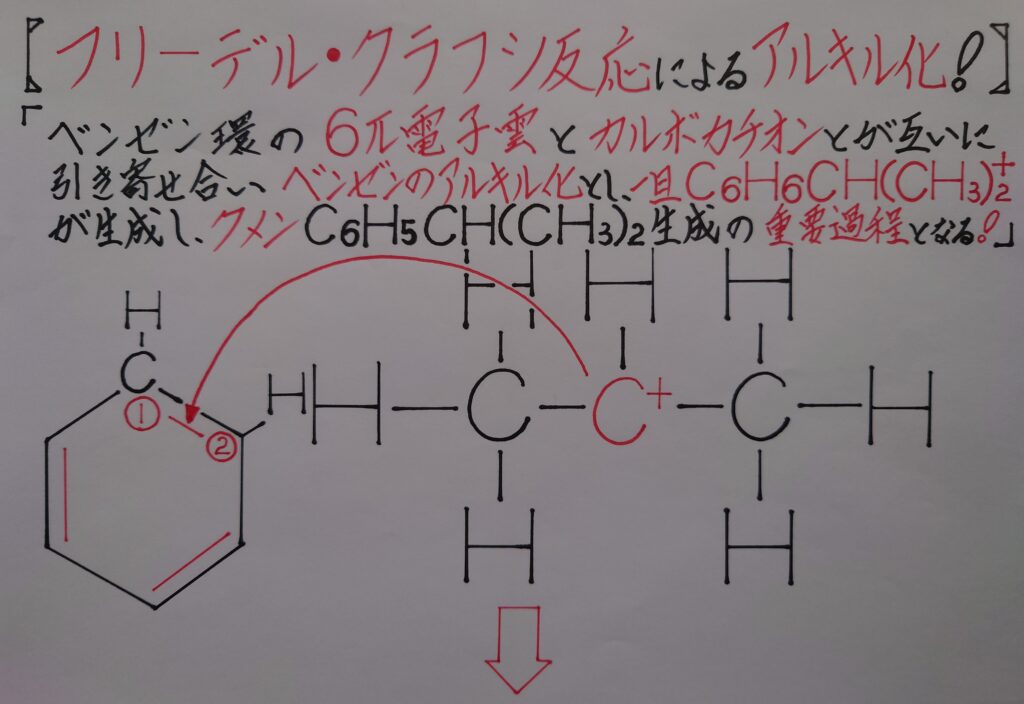

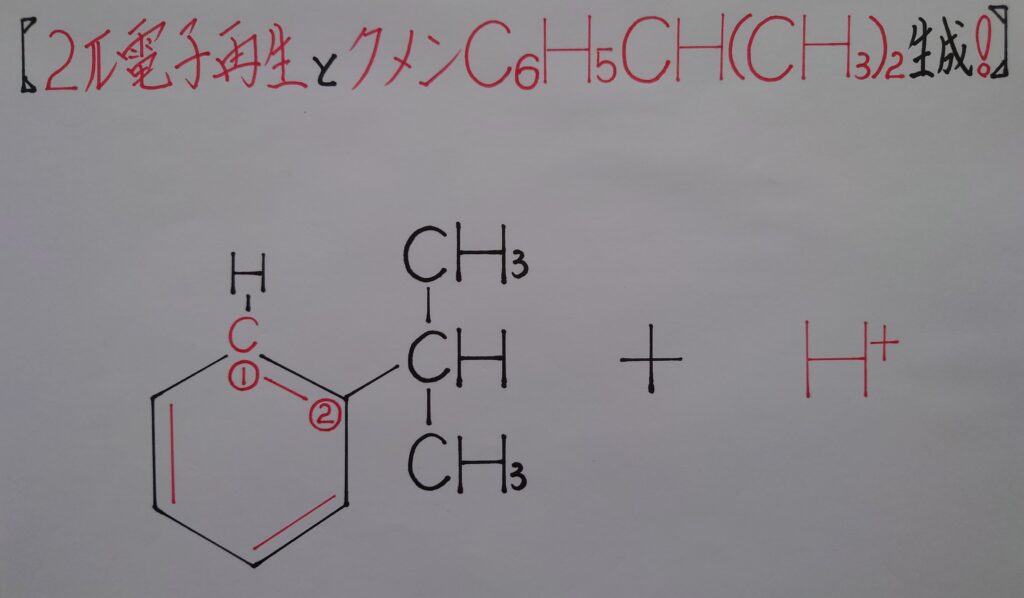
まず正電荷(+)のカルボカチオンがベンゼンの(1)の1π電子を奪うと炭素原子Cが炭素陽イオンC^+となり、直様(2)の1π電子とσ結合を形成し、イソプロピル基(❋ アルカンから1つの水素Hが外れた炭化水素基をアルキル基と呼び、ここではCH(CH3)2基です!)を導入した、一旦中間体であるC6H6CH(CH3)2^+ が生成されます。
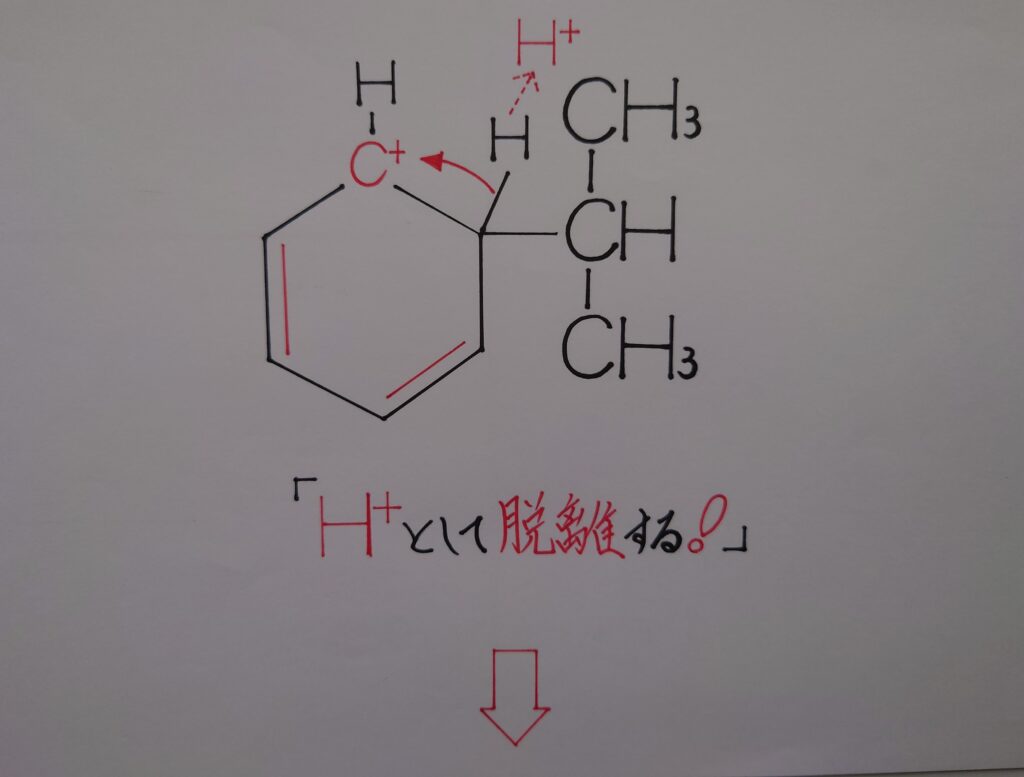
そしてイプソ位のカルボカチオンC^+が、オルト位の炭素原子Cとσ結合を形成している水素原子Hを共有電子対ごと引き寄せ1π電子を取り戻し炭素原子Cに還り、水素原子Hは水素イオンH^+として脱離します。この時Hとσ結合を形成していたオルト位の炭素原子Cの1電子が1π電子となって還り、結局2π電子の再生となりベンゼン環の6π電子雲も再生されます。
最終的にH^+脱離後は、ベンゼン環にアルキル基としてイソプロピル基が置換基となって結合した事により、結果芳香族求電子置換反応(ベンゼンのアルキル化!)によりクメンが生成します!
4.クメンラジカルから中間体の過酸化物クメンヒドロペルオキシド・C6H5C(CH3)2OOHが生成される!
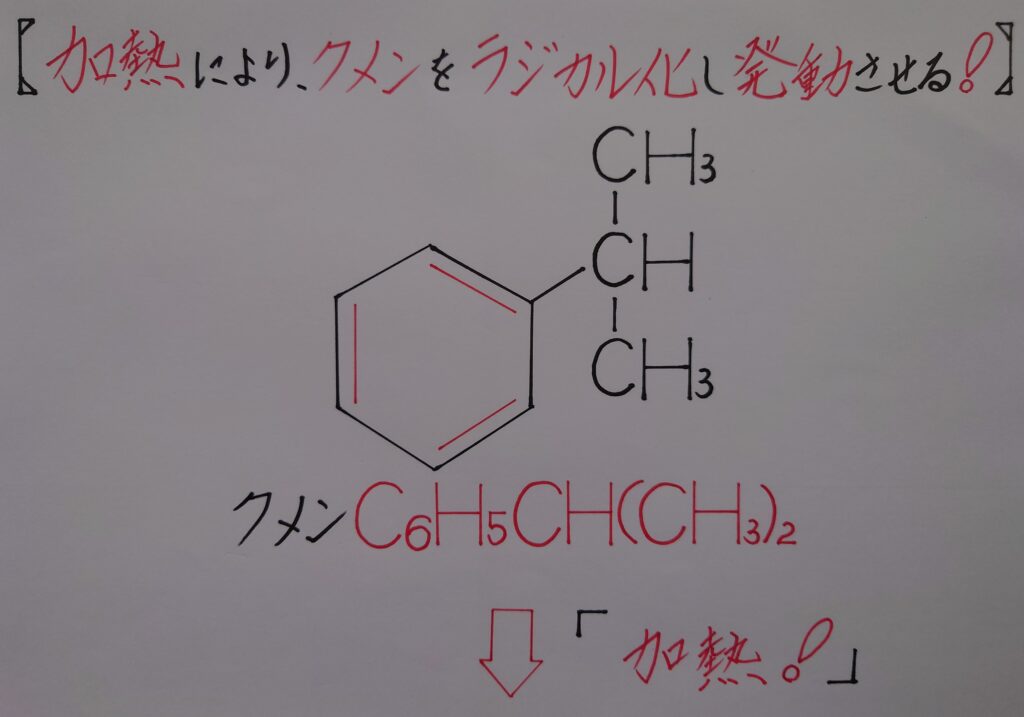
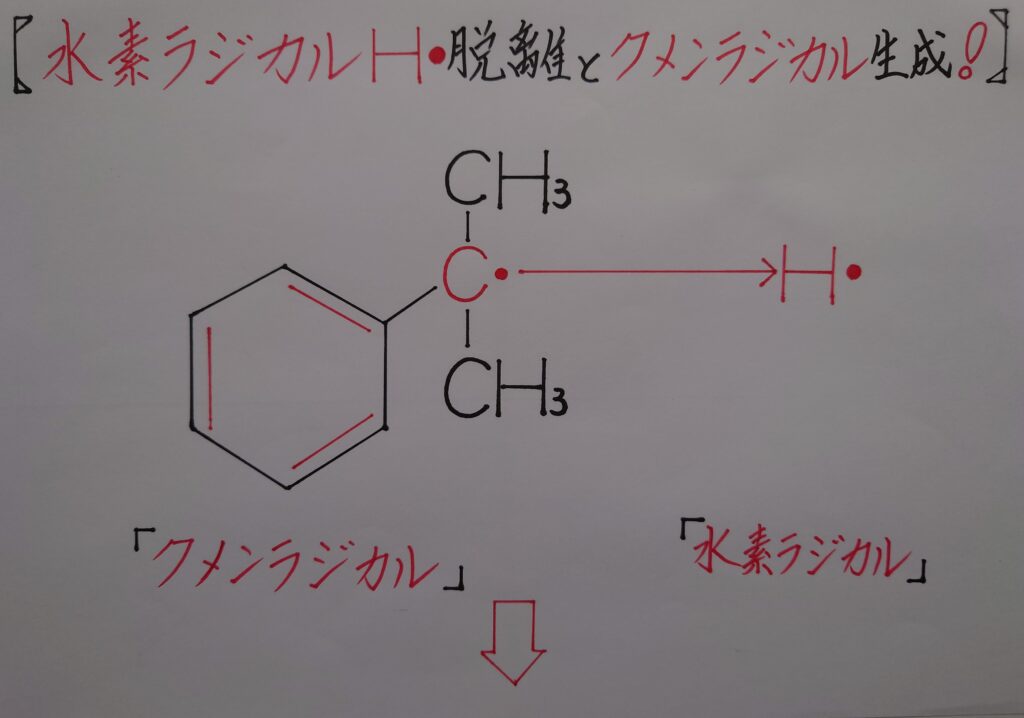
またクメンに注目して観ると、次の操作で酸素O2と結合出来る様に第3級ラジカルとして存在している事が解ります。この状態のまま酸素O2が結合しクメンを酸化する反応が起こります。
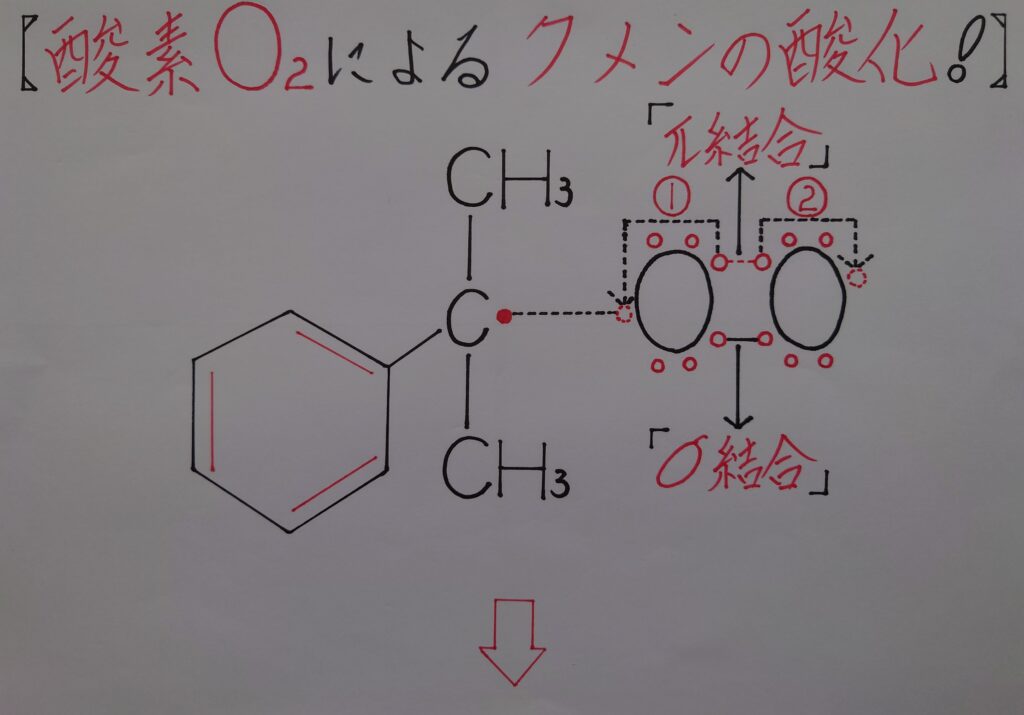
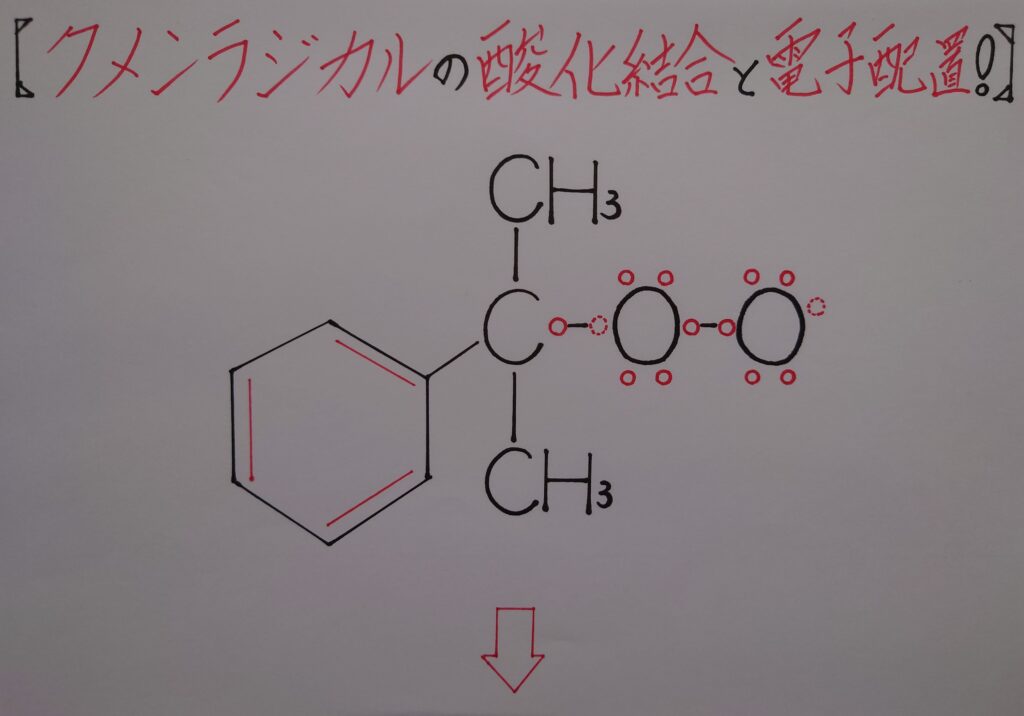
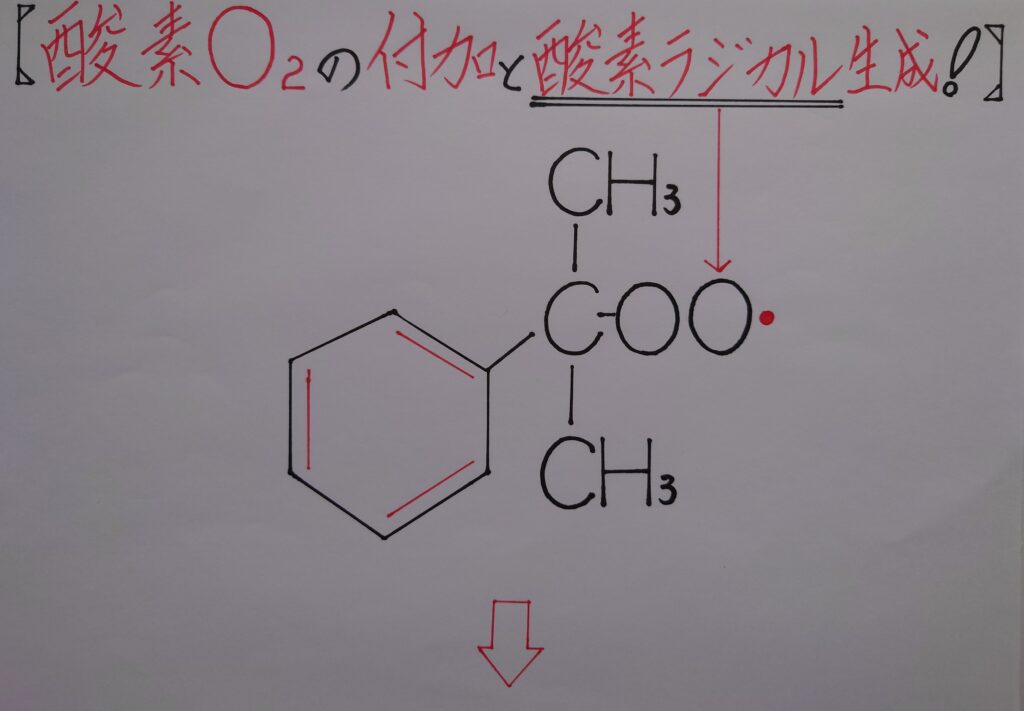
[1]クメンのラジカルがO2のπ結合の(1)の1π電子とσ結合を形成する!
[2]O2に残っている(2)の1π電子は、上図の右のO原子所有の電子となり存在し、かつ結合に不可欠な「❋ ラジカルO・」としても存在している!
[3]二重結合だったO=O結合は、σ結合(O−O結合)となりラジカルO・への結合終了となる!
この様にクメンラジカルは酸素O2のπ電子によるσ結合を形成する為、O2の右片方はラジカルO・の状態となって次の段階に進む事になります!
4−1.フル回転連鎖反応!過酸化ラジカルとクメンの反応&過酸化物クメンヒドロペルオキシドの生成!
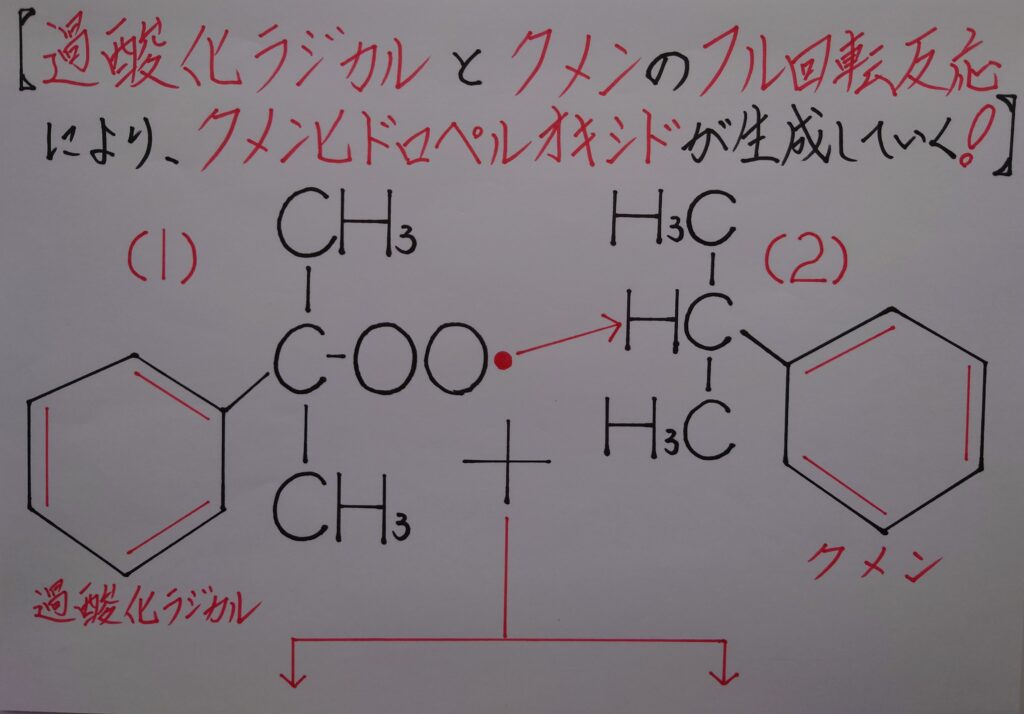
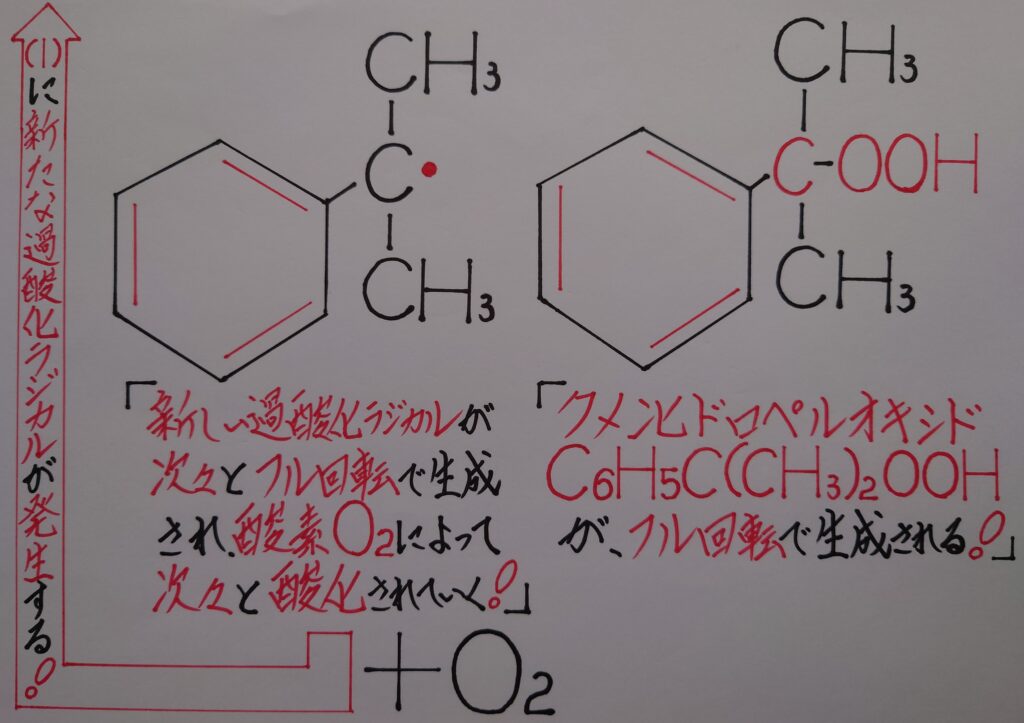
そして(2)のクメンから水素原子Hが脱離した後には新たなクメンラジカルが生成し、再び酸素O2によって酸化され(1)の新たな過酸化ラジカルが生成され(2)のクメンと反応し合い新たなクメンヒドロペルオキシドが生成する、といった様な反応がフル回転の連鎖反応によりクメンヒドロペルオキシドがどんどん量産されていく事になります!
5.中間体クメンヒドロペルオキシドと酸H^+の反応!
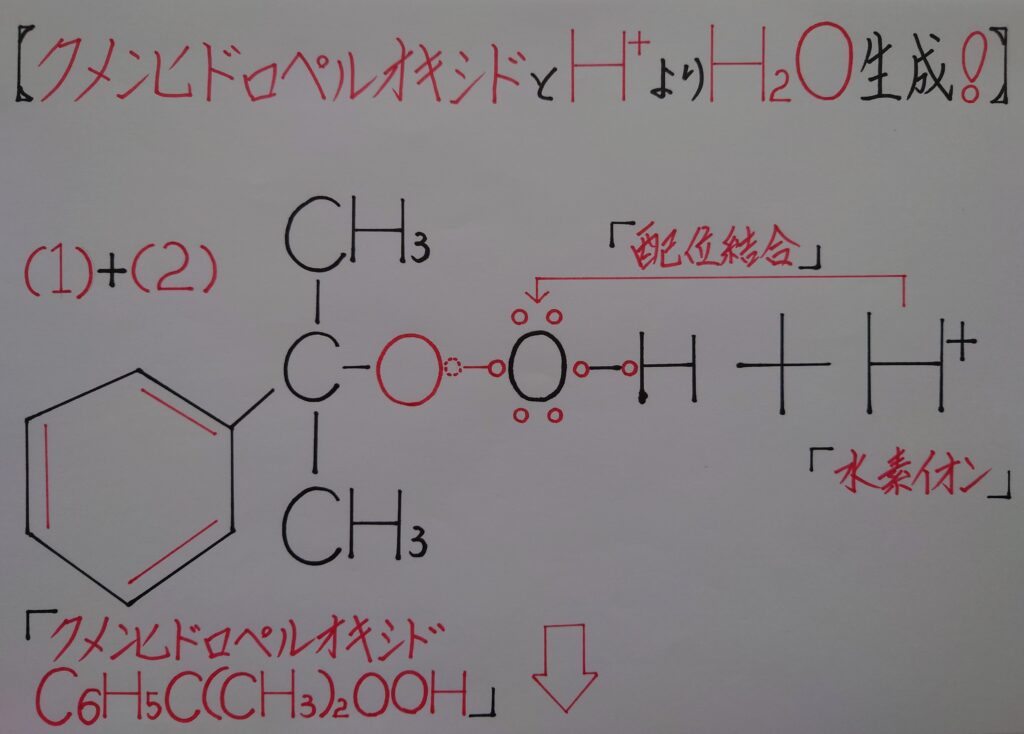
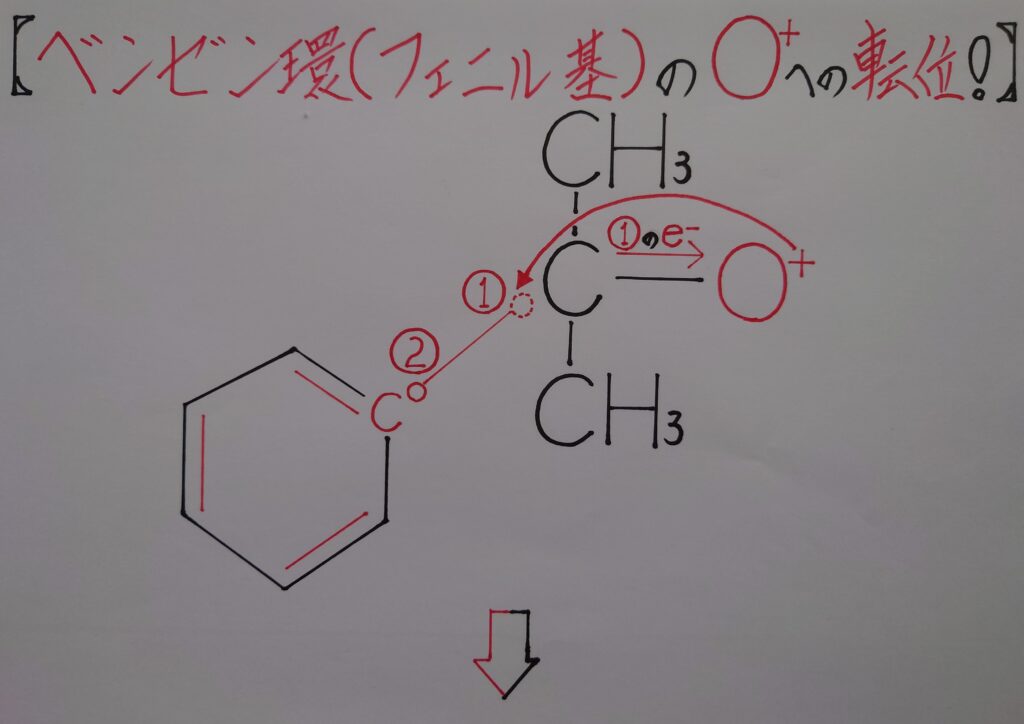
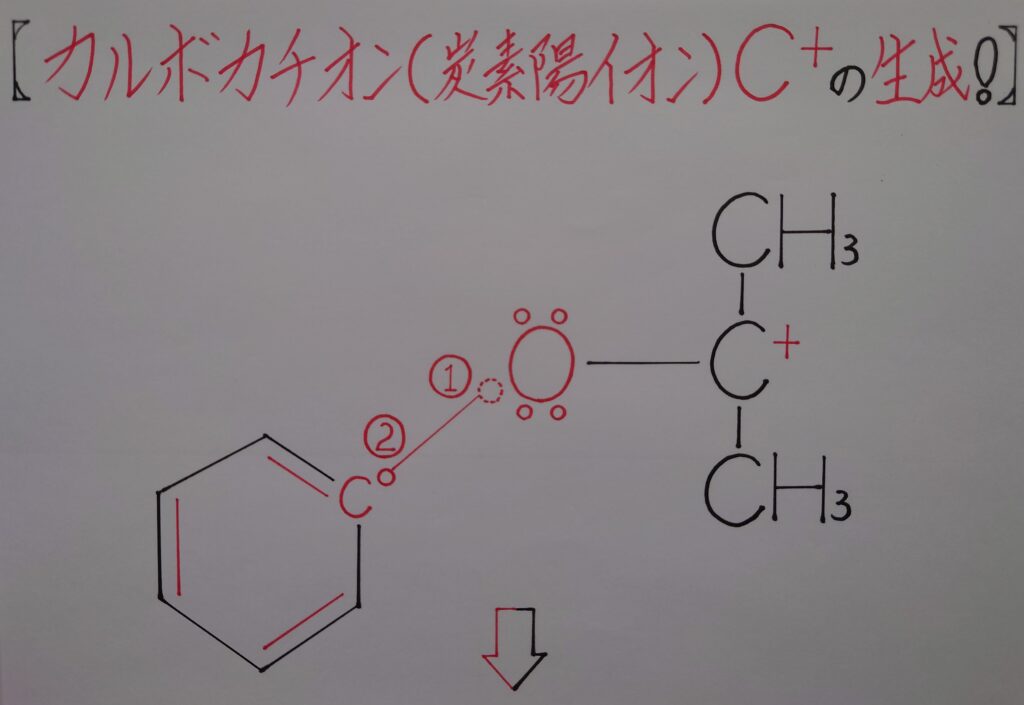
5−1.ベンゼン環(フェニル基)の酸素陽イオンO^+への転位&カルボカチオン(炭素陽イオン)C^+の生成!
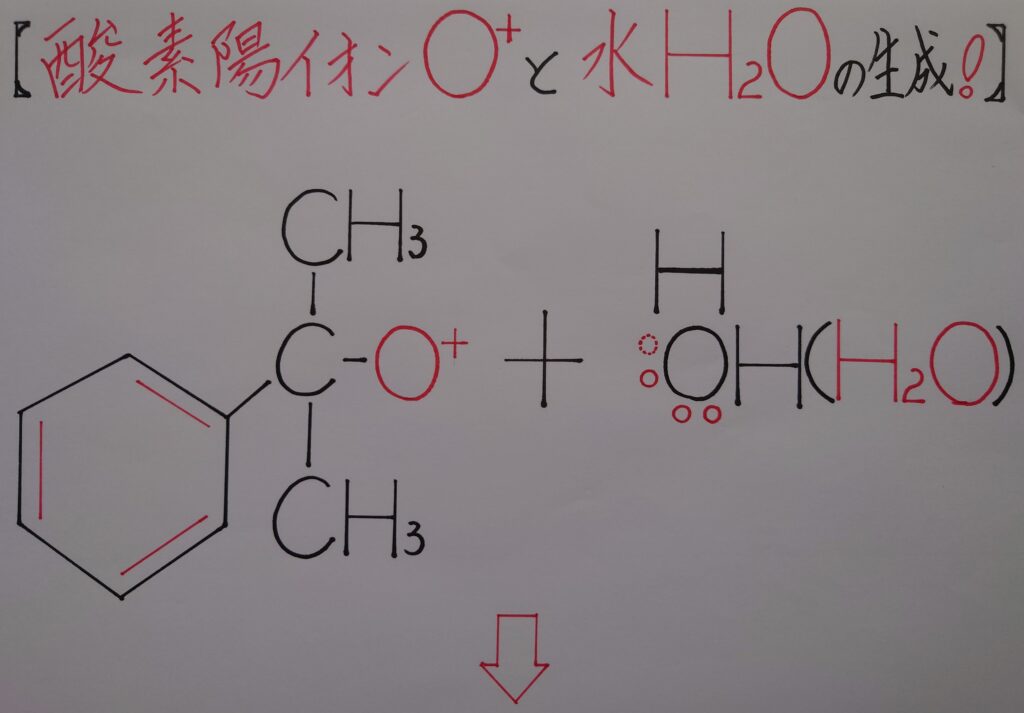
そしてこのカルボカチオンC^+と生成した水H2Oとが反応し合う事になります!
6.ヘミアセタールの形成!
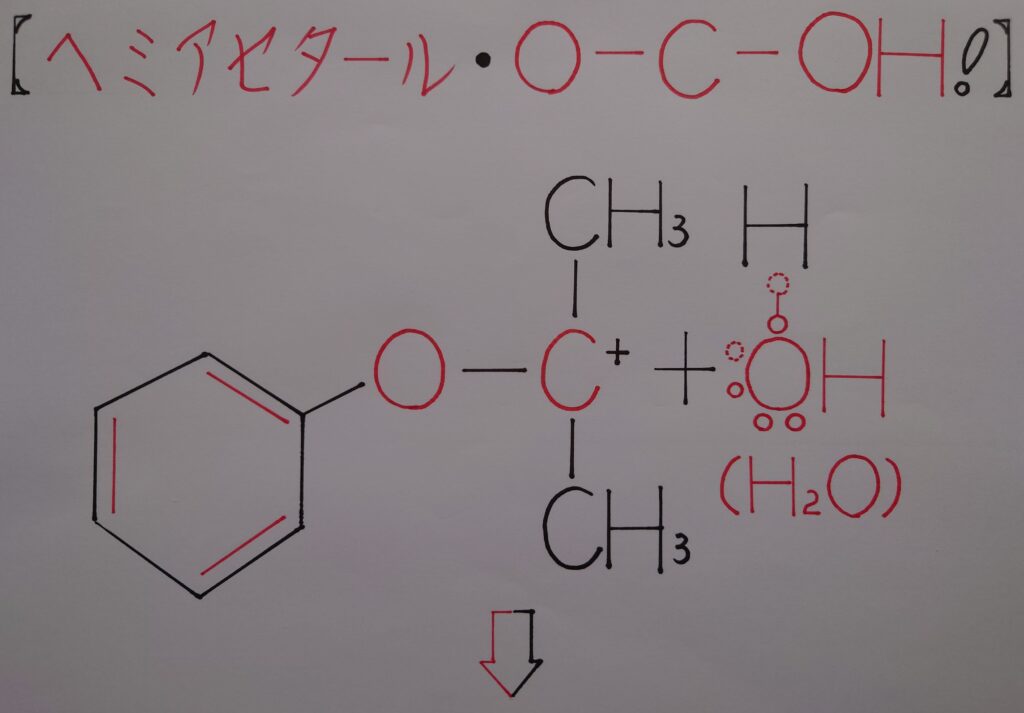
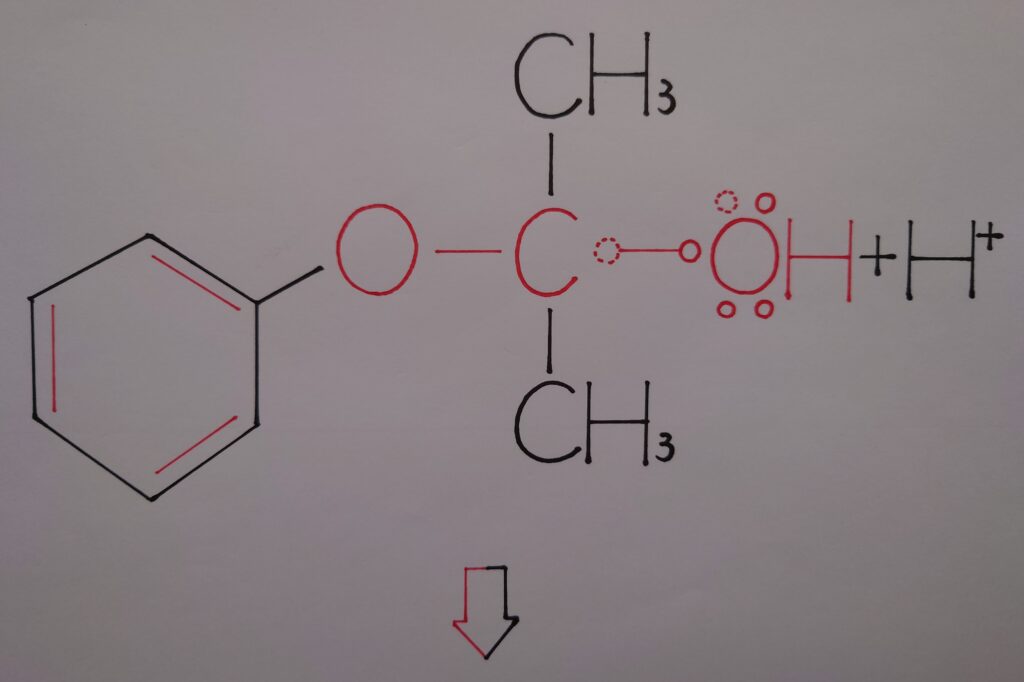
このヘミアセタールは、単糖類であるグルコース、フルクトース、ガラクトース及び二糖類のマルトース(麦芽糖)、ラクトース(乳糖)、セロビオース内にも存在しており、此等がアルデヒド基−CHOによって還元性を示す反応の過程は、フェノールとアセトンが生成する過程に良く似ていると考えられます。
また、二糖類(❋ スクロース(ショ糖)も含む!)のグリゴシド結合C−O−Cに、酸H^+を触媒とした加水分解による反応も、フェノールとアセトンが生成する過程に良く似ていると考えられます(この後どういった事かを記述しています)。
7.フェノール&アセトンが生成される2つの考え方!
通常フェノールとアセトンが生成する過程は省略されている事がありますが、ここでは私なりにフェノールとアセトンが生成する過程を予想として表してみたいと思います。
私はヘミアセタールを分解してフェノールとアセトンを生成させるには2つの考え方があるのではないかと思っています。
「1つ目は、希硫酸条件下で水素イオンH^+を作用させ加水分解により2物質として生成させ希硫酸を触媒とする。」
「2つ目は、同じく希硫酸条件下でシンプルに水素イオンH^+を作用させ触媒とする。」
以上2つの考え方でフェノールとアセトンが生成する可能性があるのではないかと思っています。実際には、いずれかの反応又は、ある比率で両者が生成するのではないかと思われますが、あくまでも予想としてのイメージを前提としていますので、よろしかったら2物質が生成される過程を御覧下さい。
7−1.フェノールとアセトンが生成される迄の過程の予想図![その1]
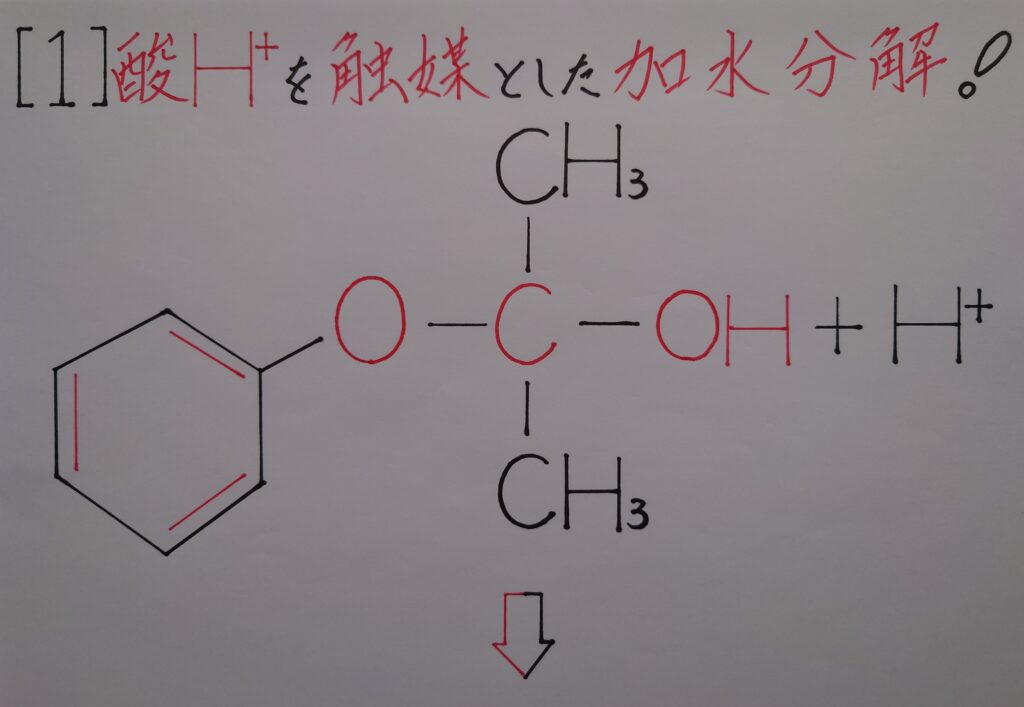
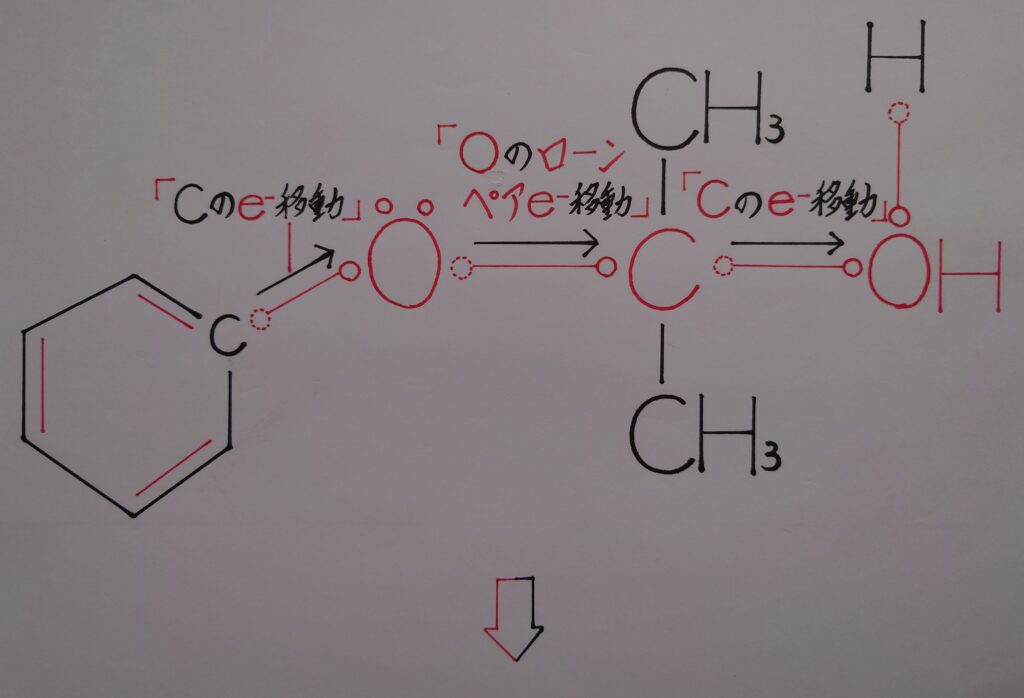
【❋ 水H2OとカルボカチオンC^+の生成!】
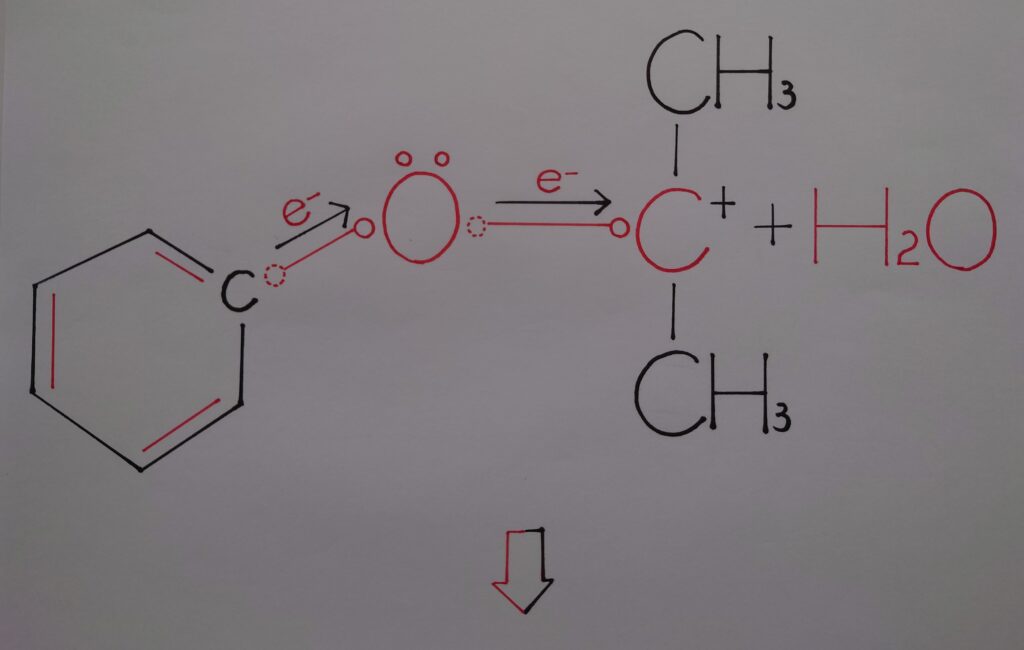
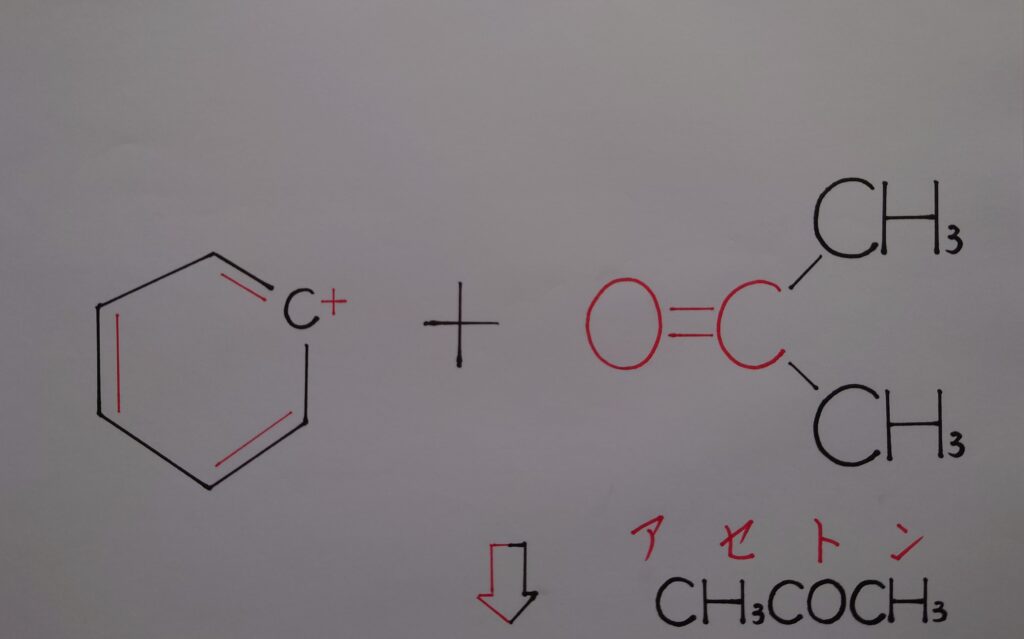
【❋ カルボカチオンC^+と水H2Oの反応!】
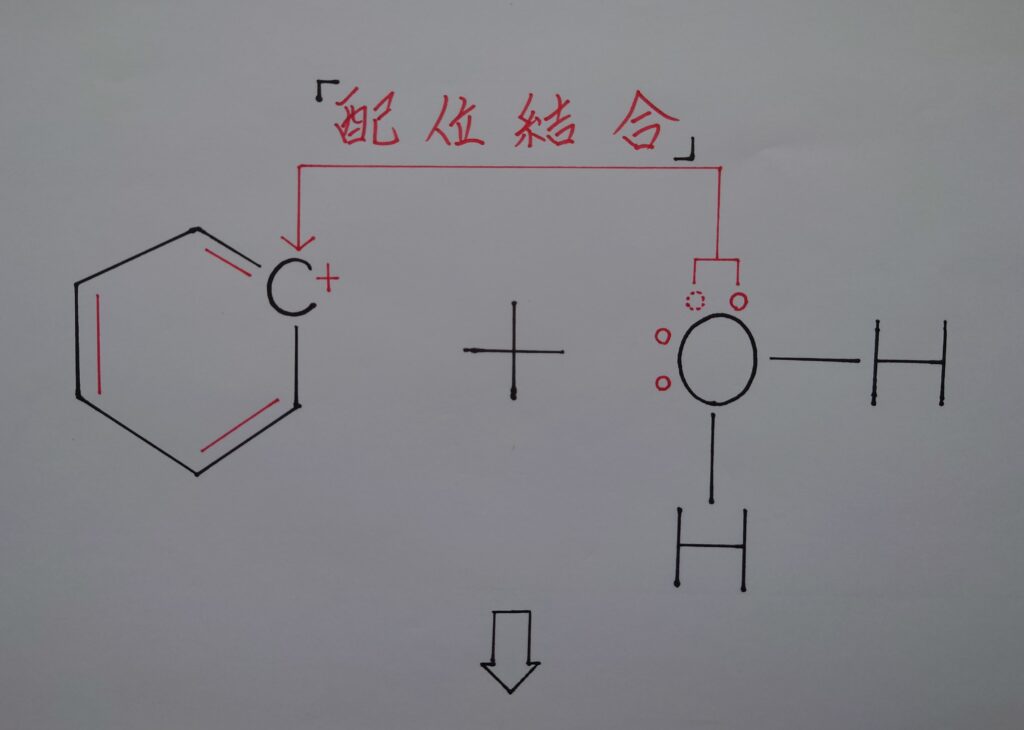
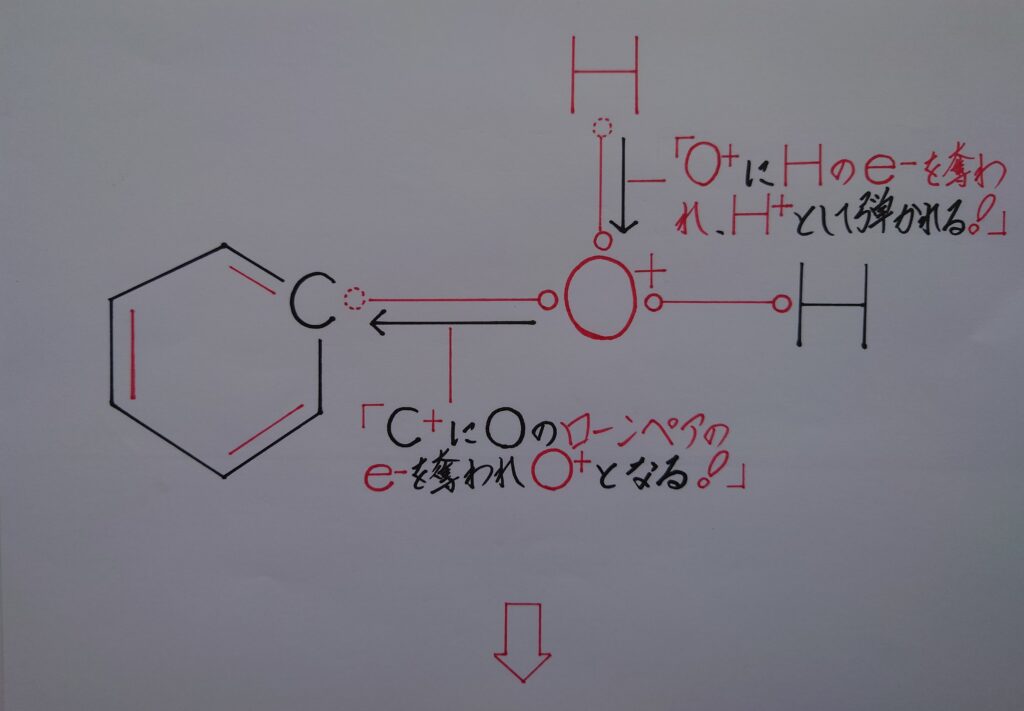
【❋ フェノールC6H5OHと水素イオンH^+の生成!】
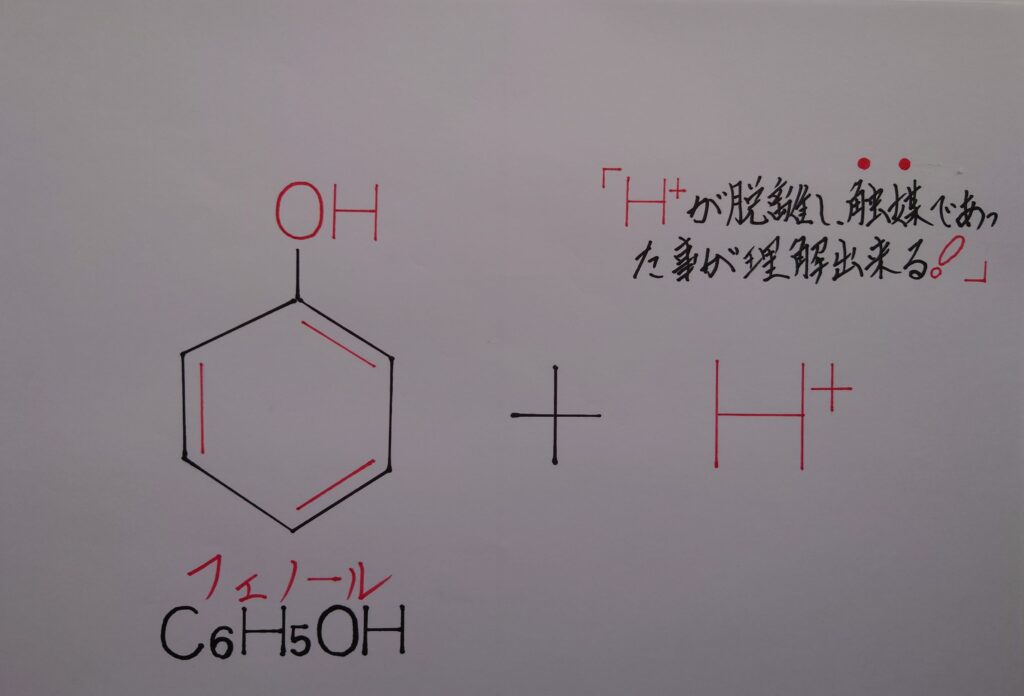
1つ目の予想はこの様に、まずアセトンCH3COCH3が生成し、次いでフェノールC6H5OHが生成されるのではないかと予想しています。
7−2.フェノールとアセトンが生成される迄の過程の予想図![その2]
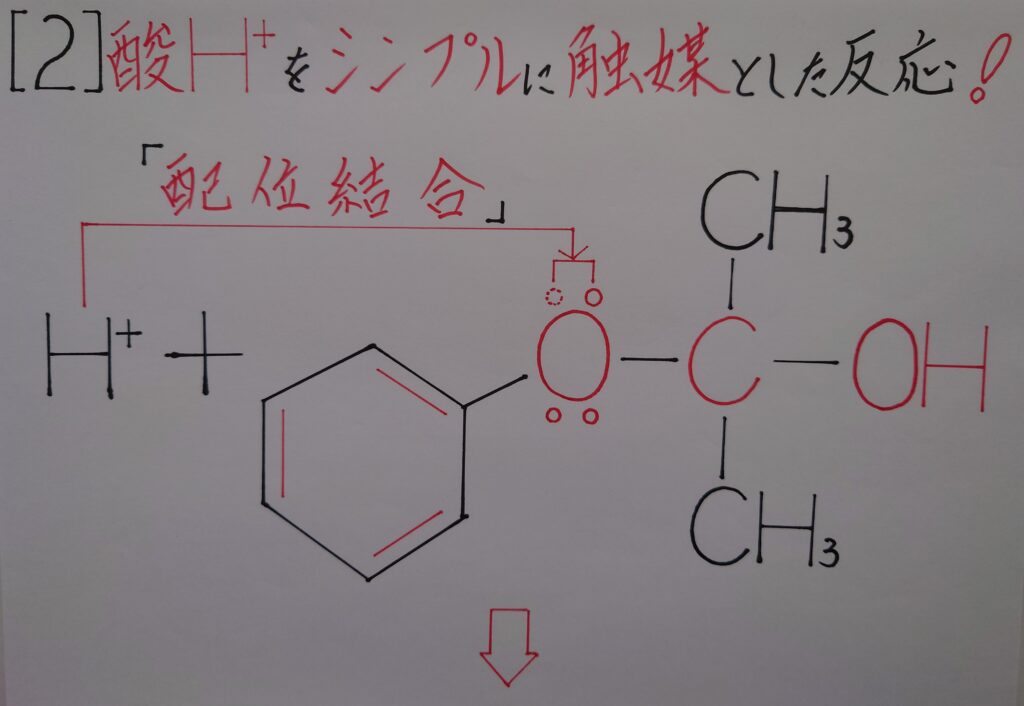
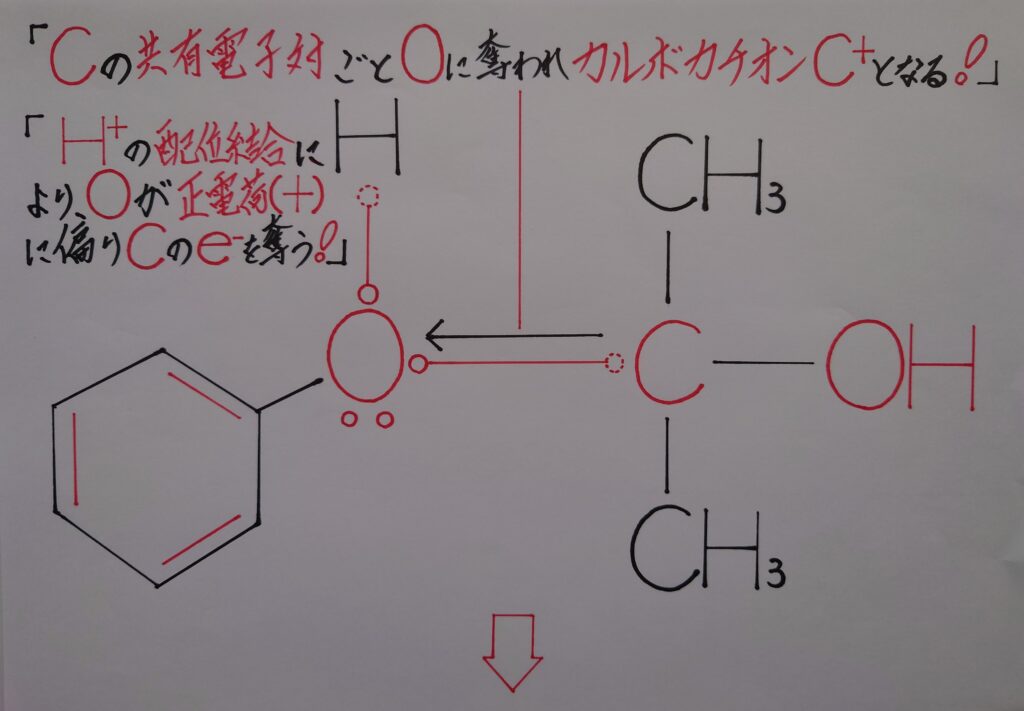
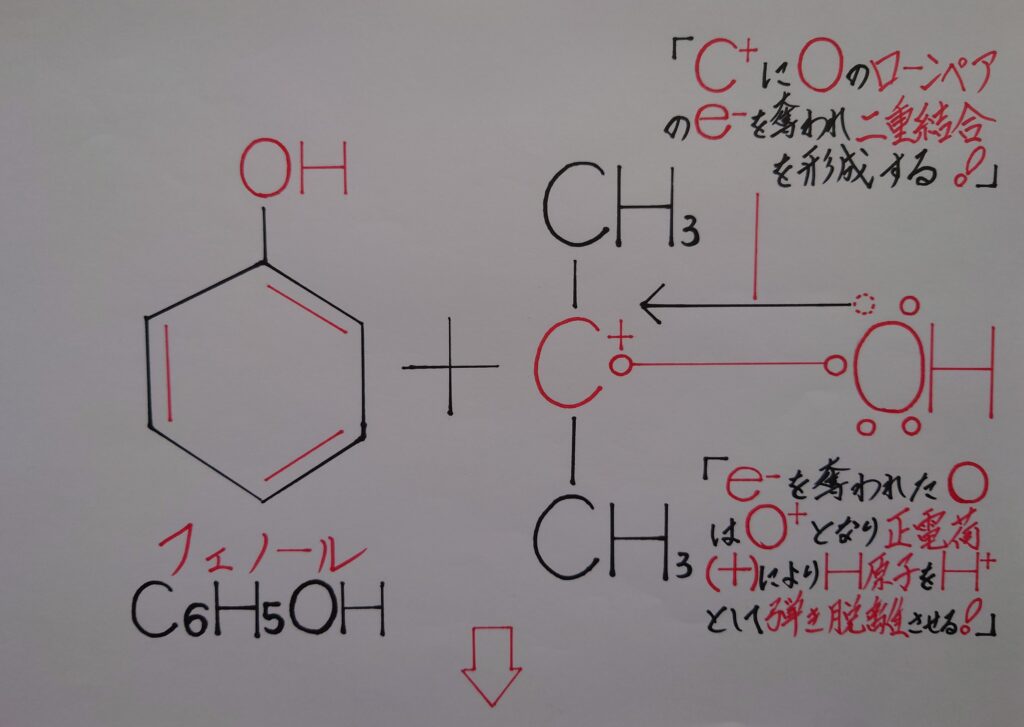
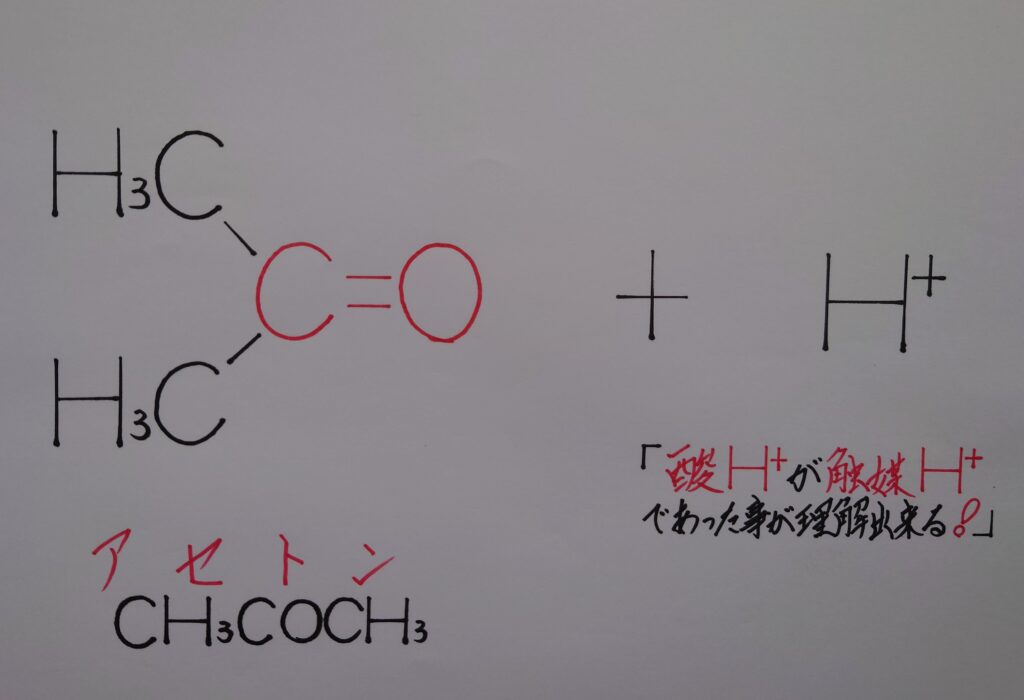
2つ目の予想は、まずフェノールが生成し、次いでアセトンが生成するのではないかと予想しています。あくまでも私の予想に過ぎませんが、1つ目と2つ目の生成の仕方とでは、フェノールとアセトンが生成する順番が真逆になるのではないかと考えられます。
さて皆さん、永々と「❋ クメン法によるフェノールとアセトンの生成!」について記述致しましたが、様々な反応を観てどんな感想を持たれたでしょうか?
「面白い!」、「複雑だけど理解出来た!」等と感じた方もいらっしゃるのではないでしょうか?今回も、やはりイメージと電子の動きを中心に考えて頂きますと理解しやすかったと思います。
【✺ 電子には混成軌道も付き物ですので、こちらの別記事の混成軌道も是非御覧下さいね!】
「必見!酢酸CH3COOHの2s軌道が電子0個になる謎とは!?」
今回は、「クメン法、改めて奥が深い!」と、うなずきながら完全させた記事となりました!
8.本物は表舞台には出て来ない!
ここからは全く関係のない話になります。うまく皆さんに伝わるか少々不安ですが、よろしかったらお付き合い下さい。
皆さんは尊敬する人はいらっしゃいますか?各々誰かしらいらっしゃるのではないでしょうか。私の尊敬する人は、継国縁壱(つぎくに・よりいち)です。そうです、「鬼滅の刃」に登場する鬼滅の剣士です!現実には存在致しませんが、「心・技・体」のいずれも兼ね備えた人物であると私自身は確信しています。
尊敬に値する人物が実際には架空であり存在しなくても、自分自身が納得した人物像であれば人生の目標になる事もあるのではないでしょうか!縁壱を知っている方々は、どの様に縁壱を捉えているでしょうか?
また架空の世界とは逆に、勿論現実社会にも尊敬する人はいますが、私は常々この様に確信しています。「❋ 本物は滅多に表舞台には出て来ない!」と。この表舞台とは目に映るテレビ等を指しています。
例えると、今コロナ禍でワクチンの接種が急を要していますが、「ワクチン、ワクチンを!」と求める事は簡単に言葉として表せますが、このワクチンの仕組みを理解されている方々が存在しているからこそ未来に希望が持てるのであって、もしこの方々が存在しなければこの先世界はどうなる事でしょうか?
私達はワクチンを提供して下さる方々を全くという程理解していないのではないでしょうか?それは、この方々が表舞台に出現する事がゼロに近い為に、また世界への貢献度が形として観えない為にワクチン供給が当たり前になっているのではないでしょうか?
他にも多数の分野ごとに、車、ロケット、新幹線、テレビ等の製造の中心人物となっておられる方々、身近に居なくてはならないお医者さん等、表舞台に出現されない人物として存在しているのではないでしょうか。
この方達は次元の異なる世界に神的存在として実在しています。私は、「世界は目に観えないこれらの貢献者によって時を刻んでいる!」と言っても過言ではないとさえ思っています。まさに常に100%でなければならず、99.999〜%では必要とされない厳しい世界に存在する方達です。
私は皆さんに形として観える人よりも、目に観えない本物の人物を捉えて、その人物の凄さを理解出来る人に成長して頂けたらと思っています。皆さんが本物を知る事により、今まで全く観えてなかった(観えるとは観察すると言う意味で扱っています!)盲点とも言うべきものに気付き新たな幅広いジャンルに対しての応用が効く様になる事でしょう。
また本物は必ず化学と関係共通していますので、本物を知る事により、一層化学の世界に興味を魅かれる事でしょう!そして改めて「❋ 本物を知る!」って重要だと痛感される事でしょう!
今回のクメン法に関しても、クメン法を編出した本物が存在したからこそ、私達はその凄さに気付く事が出来、学ぶ事が出来ています。またまた改めて「❋ クメン法って凄いですね!」。
皆さん、今回も永々ご静聴有難う御座いました!次回も「本物だな!」って思って頂ける記事に挑戦致しますので、宜しくお願い致します!それでは、この辺で、See you!




















